Giải bài 4 Phản ứng trao đổi ion trong dung dịch các chất điện li
Tech12h xin gửi tới các bạn bài phản ứng trao đổi ion trong dung dịch các chất điện li. Bài đăng giúp bạn hiểu bản chất, điều kiện xảy ra phản ứng trao đổi ion trong dung dịch chất điện li. Ngoài ra viết được phương trình ion rút gọn của phản ứng. Mong các bạn tham khảo!
A - Kiến thức trọng tâm
I. Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch chất điện li
1.Phản ứng tạo thành kết tủa
- Phương trình ion rút gọn cho biết bản chất của phản ứng trong dung dịch các chất điện li.
- Cách chuyển phương trình dưới dạng phân tử thành phương trình ion rút gọn như sau
- Chuyển tất cả chất vừa dễ tan, vừa điện li mạnh thành ion.
- Các chất khí, kết tủa, điện li yếu để nguyên dưới dạng phân tử.
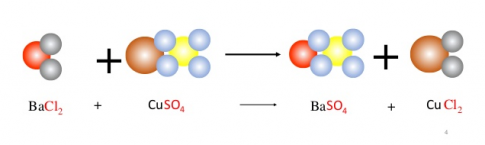
Ví dụ: 2Na+ + SO42- + Ba2+ + Cl- → BaSO4↓ + 2Na+ + 2Cl-
Rút gọn: Ba2+ + SO42- → BaSO4↓
- Muốn điều chế kết tủa BaSO4 cần trộn hai dung dịch một dung dịch chứa Ba2+ , dung dịch kia chứa SO42-
2.Phản ứng tạo thành chất điện li yếu
a.Phản ứng tạo thành nước
- Phương trình ion thu gọn
H+ + OH- → H2O
Ví dụ: NaOH + HCl → NaCl + H2O
- Phản ứng giữa dung dịch axit và hidroxit có tính bazơ rất dễ xảy ra vì tạo thành nước.
b.Phản ứng tạo thành axit yếu
- Trong dung dịch ion H+ sẽ kết hợp với các ion có tính bazơ yếu để tạo thành axit yếu
Ví dụ: HCl và CH3COONa ta được phương trình ion thu gọn:
H+ + CH3COO- → CH3COONa
2.Phản ứng tạo thành chất khí
- Phản ứng giữa muối cacbonat và dung dịch axit rất dễ xảy ra vì vừa tạo thành chất điện li yếu là H2O , vừa tạo ra chất khí CO2 tách khỏi môi trường phản ứng
- Phương trình ion thu gọn:
2H+ + CO32- → CO2 + H2O
II.Kết luận
1. Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
2. Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất một trong các chất sau:
- Chất kết tủa.
- Chất điện li yếu.
- Chất khí.
Nội dung quan tâm khác
Giải bài tập những môn khác
Giải sgk lớp 11 kết nối tri thức
Giải sgk lớp 11 chân trời sáng tạo
Giải sgk lớp 11 cánh diều
Giải SBT lớp 11 kết nối tri thức
Giải SBT lớp 11 chân trời sáng tạo
Giải SBT lớp 11 cánh diều
Giải chuyên đề học tập lớp 11 kết nối tri thức
Giải chuyên đề toán 11 kết nối tri thức
Giải chuyên đề ngữ văn 11 kết nối tri thức
Giải chuyên đề vật lí 11 kết nối tri thức
Giải chuyên đề hóa học 11 kết nối tri thức
Giải chuyên đề sinh học 11 kết nối tri thức
Giải chuyên đề kinh tế pháp luật 11 kết nối tri thức
Giải chuyên đề lịch sử 11 kết nối tri thức
Giải chuyên đề địa lí 11 kết nối tri thức
Giải chuyên đề mĩ thuật 11 kết nối tri thức
Giải chuyên đề âm nhạc 11 kết nối tri thức
Giải chuyên đề công nghệ chăn nuôi 11 kết nối tri thức
Giải chuyên đề công nghệ cơ khí 11 kết nối tri thức
Giải chuyên đề tin học 11 định hướng Khoa học máy tính kết nối tri thức
Giải chuyên đề tin học 11 định hướng Tin học ứng dụng kết nối tri thức
Giải chuyên đề quốc phòng an ninh 11 kết nối tri thức
Giải chuyên đề hoạt động trải nghiệm hướng nghiệp 11 kết nối tri thức
Giải chuyên đề học tập lớp 11 chân trời sáng tạo
Giải chuyên đề học tập lớp 11 cánh diều
Trắc nghiệm 11 Kết nối tri thức
Trắc nghiệm 11 Chân trời sáng tạo
Trắc nghiệm 11 Cánh diều
Bộ đề thi, đề kiểm tra lớp 11 kết nối tri thức
Đề thi Toán 11 Kết nối tri thức
Đề thi ngữ văn 11 Kết nối tri thức
Đề thi vật lí 11 Kết nối tri thức
Đề thi sinh học 11 Kết nối tri thức
Đề thi hóa học 11 Kết nối tri thức
Đề thi lịch sử 11 Kết nối tri thức
Đề thi địa lí 11 Kết nối tri thức
Đề thi kinh tế pháp luật 11 Kết nối tri thức
Đề thi công nghệ cơ khí 11 Kết nối tri thức
Đề thi công nghệ chăn nuôi 11 Kết nối tri thức
Đề thi tin học ứng dụng 11 Kết nối tri thức
Đề thi khoa học máy tính 11 Kết nối tri thức
Bộ đề thi, đề kiểm tra lớp 11 chân trời sáng tạo
Bộ đề thi, đề kiểm tra lớp 11 cánh diều
Đề thi Toán 11 Cánh diều
Đề thi ngữ văn 11 Cánh diều
Đề thi vật lí 11 Cánh diều
Đề thi sinh học 11 Cánh diều
Đề thi hóa học 11 Cánh diều
Đề thi lịch sử 11 Cánh diều
Đề thi địa lí 11 Cánh diều
Đề thi kinh tế pháp luật 11 Cánh diều
Đề thi công nghệ cơ khí 11 Cánh diều
Đề thi công nghệ chăn nuôi 11 Cánh diều
Đề thi tin học ứng dụng 11 Cánh diều
Đề thi khoa học máy tính 11 Cánh diều

Bình luận