Giải bài 19 Tốc độ phản ứng
Giải bài 19 Tốc độ phản ứng - Sách hóa học 10 kết nối tri thức. Phần đáp án chuẩn, hướng dẫn giải chi tiết cho từng bài tập có trong chương trình học của sách giáo khoa. Hi vọng, các em học sinh hiểu và nắm vững kiến thức bài học.
I. Tốc độ phản ứng hóa học
Câu 1. Xét phản ứng: H2+Cl2→2HCl
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị sau:
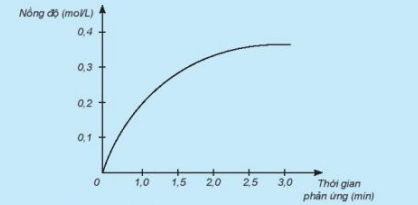
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
b) Nêu đơn vị của tốc độ phản ứng trong trường hợp này
Trả lời:
a) Đồ thị mô tả sự thay đổi nồng độ theo thời gian của HCl.
b) Đơn vị của tốc độ phản ứng: mol/L.min
Nội dung quan tâm khác
Từ khóa tìm kiếm: giải hóa 10 kết nối tri thức, giải sách kết nối tri thức 10 môn hóa, giải hóa 10 sách mới bài 19,bài 19 Tốc độ phản ứng.
Bình luận